来源:源达 投资要点 医美再生抗衰注射剂是新兴上市材料,实现面部年轻化 再生抗衰类材料有别于玻尿酸类和肉毒素类的原因在于:(i). 作用机制不同:再生抗衰类产品的共同机制是通过补充或刺激产生胶原蛋白等各种通路从而起到抗衰效果;(ii). 实现效果不同:再生抗衰类产品的共同效果是实现面部年轻化;(iii). 材料出现时间不同:再生抗衰类材料是国内市场近年来新兴上市材料。 再生抗衰注射剂产业中游是行业附加值最大环节 产业链中游为行业附加值最大环节,目前政策合规要求、技术革新与自主研发能力、规模化生...
来源:源达
投资要点
医美再生抗衰注射剂是新兴上市材料,实现面部年轻化
再生抗衰类材料有别于玻尿酸类和肉毒素类的原因在于:(i). 作用机制不同:再生抗衰类产品的共同机制是通过补充或刺激产生胶原蛋白等各种通路从而起到抗衰效果;(ii). 实现效果不同:再生抗衰类产品的共同效果是实现面部年轻化;(iii). 材料出现时间不同:再生抗衰类材料是国内市场近年来新兴上市材料。
再生抗衰注射剂产业中游是行业附加值最大环节
产业链中游为行业附加值最大环节,目前政策合规要求、技术革新与自主研发能力、规模化生产能力以及不断变化的市场需求,共同构筑了产业链中游的发展壁垒。
消费者对机构或医生的专业性考量、医美机构的客户留存与拓新是下游市场最大痛点,近年中游厂商通过KOL教育不断增强中下游协同性,利于提高注射医生水平的同时及时获得临床反馈,实现全产业链良性闭环。
医美再生抗衰注射剂行业未来发展趋势
需求端:人口老龄化提振的抗衰需求、非手术类医美是中高收入医美消费者的主流项目选择、消费者美学观念向轻量化项目转变以及对注射部位的需求转变,将推动生产企业在开发注射剂产品时,更关注功能及功效。
供给端:新技术和新材料的迭代与出现,将提供在胶原蛋白生成速度、维持时效、可降解性以及个性化定制等方面优势的注射剂产品,未来有望逐步替代传统医美注射材料的部分市场空间。
投资建议
在趋于严格的行业合规与市场监管、较高壁垒的研发创新与规模化生产等市场痛点下,具有“合规化”基因,研产销全产业链布局,丰富产品布局的企业有望屹立快速发展的行业潮头,展现较强的发展潜力和投资价值。建议关注: 1)锦波生物;2)华东医药。
风险提示
政策变动风险;行业竞争加剧;新品研发不及预期。
一、中国医美再生抗衰注射剂行业综述
医美注射剂产品定义及分类医美注射剂通常由注射器以及预装载于注射器或安瓿瓶中的玻尿酸类、肉毒素类以及再生抗衰类的材料组成。中国根据作用机制、实现效果及材料出现时间,医美注射剂产品可被分为玻尿酸类、肉毒素类以及再生抗衰类,再生抗衰类有别于玻尿酸类和肉毒素类的原因在于 (i). 作用机制不同:再生抗衰类产品的共同机制是通过补充或刺激产生胶原蛋白等各种通路从而起到抗衰效果;(ii). 实现效果不同:再生抗衰类产品的共同效果是实现面部年轻化;(iii). 材料出现时间不同:再生抗衰类材料是国内市场近年来新兴上市材料。
玻尿酸类:学名为透明质酸,是一种细胞外基质成分,广泛分布在人和动物体内的真皮、晶状体、关节软骨等组织中;其被作为组织填充剂注射至面部组织内,可以起到支撑填充的作用,并且由于材料特性,可以达到面部凹陷填充、皮肤补水等目的。
肉毒素类:一种由肉毒杆菌分泌的神经毒素,分为多个型别,目前最常用于临床和医美治疗的为A型;通过阻断神经和肌肉间的信号传导,以放松肌肉、减小肌肉体积,达到局部除皱、瘦脸、瘦腿等目的。
再生抗衰类:再生抗衰类注射剂又分为微球再生类、胶原蛋白类、PDRN类以及其他包括外泌体、托细胞外基质、PRP等类别。具体来看,1)微球再生类:一种以生物刺激性材料为主要成分,按主要成分可分为PLLA、PDLLA、PCL、CaHA等,通过刺激人体自身免疫反应来促进胶原蛋白的再生,从而起到增容、紧致、抗衰等目的。2)胶原蛋白类:是一种生物聚合物,在体内以三股螺旋结构组成胶原,而胶原又堆叠成纤维或非纤维结构,通过注射到真皮层或皮下组织,刺激胶原再生,从而达到皱纹填充、皮肤美容等目的。3)PDRN类:天然来源的DNA衍生物,由链长50~2,000个碱基对的DNA片段的混合物组成,最初被描述为一种从人胎盘中提取的组织修复刺激剂,目前主要从鲑鱼的精子细胞中提取和纯化,基于PDRN成分的安全有效性,已有大量研究积累,证明其具有解决炎症性皮肤问题、修复皮肤创面、对抗皮肤老化、实现胶原再生等功效。
2.医美再生抗衰注射剂的作用机制与优势
主要以胶原蛋白类、微球再生类和PDRN类材料为主,通过刺激人体自身胶原蛋白的再生从而起到美容抗衰的作用,具有在胶原蛋白生成速度、维持时效、可降解性以及个性化定制等方面的优势。
|
图1:医美再生抗衰注射剂的产品分类 |

|
|
资料来源:弗若斯特沙利文,源达信息证券研究所 |
3.医美再生抗衰注射剂行业发展历程
3月11日在技术迭代推动了新材料研发、产品制备工业化进程加速的影响下,诸多国产厂商如锦波生物、吴中美学、华东医药在微球再生类、PDRN类等领域的先发性布局,有望引领医美再生抗衰注射剂行业迈入爆发。
医美再生抗衰注射剂行业的历程可大致分为行业萌芽期(20世纪前至2008年)、行业发展期(2009-2020年)以及行业爆发期(2021年至今)三个阶段。
行业萌芽期:随着对原材料的发现、制备工艺和技术的探索加深,医美再生抗衰注射剂行业的工业化、商业化的步伐不断加快;胶原蛋白等产品的率先上市,也逐步验证其在医美领域的治疗效果。
行业发展期:各国和地区相继获批了产品的多种适应症,代表认可其市场地位和作用优势;此外,国产企业加速收购、研发步伐,推动行业实现快速发展。
行业爆发期:国产企业的技术实力涌现,加速推进各类国内“首款”产品的商业化进程,行业进入快速爆发期,中国企业的国际影响力不断加大。
图2:医美再生抗衰注射剂行业发展历史

资料来源:弗若斯特沙利文,源达信息证券研究所
4.中国医美注射剂市场规模及潜在增长空间预测
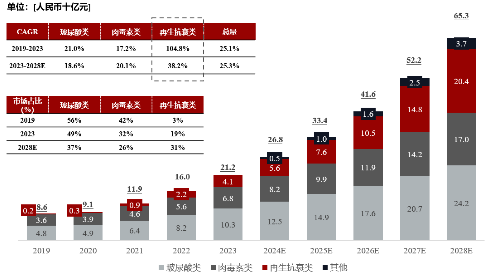
以出厂价计,2023年中国医美注射剂市场规模达212亿元人民币,预计2028年将增加至653亿元人民币,期间年复合增长率为25.3%;其中,再生抗衰类的市场占比将从2019年的3%,预计于2028年增至31%。
图3: 中国医美注射剂市场规模及潜在增长空间预测,2019-2028E
资料来源:弗若斯特沙利文,源达信息证券研究所
再生抗衰类是医美注射剂所有材料中,增速最快的细分市场。2023年,再生抗衰类市场规模为40.5亿元人民币,预计到2028年的市场年复合增速为38.2%将远超同期的总体市场、玻尿酸类和肉毒素类市场。
再生抗衰类的市场占比逐步提升,有望替代部分老材料。由于目前中国市场:1)与填充塑形的需求相比,再生抗衰的需求更具备普适性,目标受众更大,在老龄化的背景下将逐渐成为主流趋势;2)美学观念的变化,从以前更追求轮廓塑形,转变为更自然的审美,消费者倾向于轻量化的项目;3)老材料逐步浮现出一些问题,例如玻尿酸打多出现馒化、交联剂残留等,因此再生抗衰类材料在胶原蛋白生成速度、维持时效、可降解性以及个性化定制等方面的优势,将推动其未来替代一部分老材料的市场规模。
5.中国医美再生抗衰注射剂市场规模及潜在增长空间预测
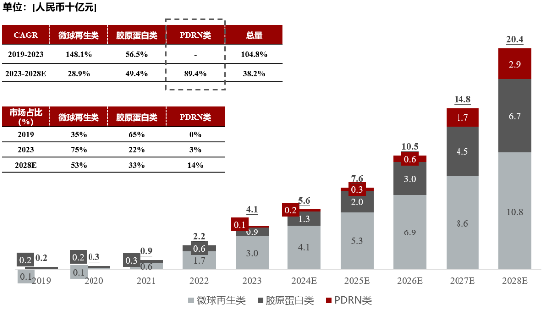
以出厂价计,2023年中国医美再生抗衰注射剂市场规模达41亿元人民币,预计2028年将增加至204亿元人民币,胶原蛋白类以及PDRN类将分别占比53%、33%、14%。
图4:中国医美再生抗衰注射剂市场规模及潜在增长空间预测,2019-2028E
资料来源:弗若斯特沙利文,源达信息证券研究所
微球再生类是目前及未来最大的细分市场。微球再生类在2019年的市场规模为0.8亿元人民币,在医美再生抗衰注射剂市场占比为35%。随着新产品不断上市,2023年,其市场规模增至为30.3亿元人民币,市场占比增至75%。预计2028年,市场规模将进一步增长至107.7亿元人民币。
PDRN类材料目前仍是空白市场,但行业未来的潜在增速较高。目前国内有部分非合规的PDRN注射产品在销售,但尚无合规的三类器械产品。因此参考海外尤其是韩国市场的发展来看,随着未来国内合规产品的上市,PDRN材料将在医美市场占据显著份额。预计23-28年市场年复合增速为89.4%,将超过同期市场总量的38.2%增速。
二、中国医美再生抗衰注射剂产业链分析
1.产业链图谱
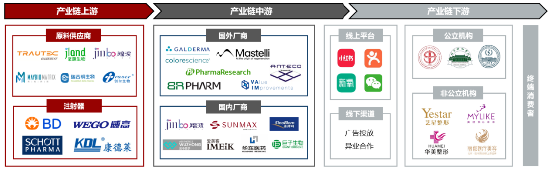
医美再生抗衰注射剂产业链上游为原料及注射器厂商,最终被制成注射剂的形式,通过线上及线下渠道供给下游终端客户,其中产业链中游为行业附加值最大环节。
图5:中国医美再生抗衰注射剂产业链图谱
资料来源:弗若斯特沙利文,源达信息证券研究所
各环节议价能力:
中游: (i). 注射剂生产商通过将原料制成微球再生类、胶原蛋白类和PDRN类注射剂,是产业链附加值最大环节,议价能力强; (ii). 日前中游厂商主要以自主研发、收购或产品许可引进的方式进入市场,近年随着技术实力的突破、国产替代政策的影响,本土厂商实力逐步涌现。 下游: (i). 中游厂商凭借积累的产业资源与资金优势,以直营的模式延伸业务条线至下游医美机构; (ii). 未来产业链中下游的协同性将进一步加强,将通过医生教育以增强注射医生对材料特性的掌握,以及注射水平的提升。2.产业链上游分析
原料及注射器的质量决定了注射剂的疗效和安全性,近年头部厂商通过创新制备技术、新型材料、精密制造工艺等手段,加强其在产业链环节中的议价能力和竞争壁垒。
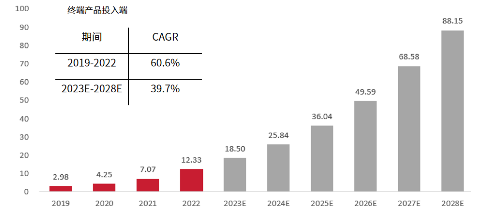
以重组胶原蛋白原料为例,其质量直接决定了注射剂的疗效和安全性,创新技术的发展使原料合成和提纯更精细。目前快速发展的中国医美再生抗衰注射剂行业,也将增加对上游原料的市场需求。当前具备优质原料生产能力的企业,因较强的议价能力,已有如巨子生物、聚源生物等企业,开始向产业链中游延伸布局,未来产业链一体化将会是企业用来增强市场竞争力以获取更高市场份额和商业回报的手段。
图6:中国重组胶原蛋白原料市场规模
资料来源:弗若斯特沙利文,源达信息证券研究所
医用注射器的注意要点:1)需防止注射剂因光照、冻融、水蒸气、氧气等活性气体以及微生物污染而造成的产品质量下降;2)应具备良好的透明度和物理强度,确保在使用过程中不易变形或破裂;3)此外还应具有良好的化学稳定性,不易与药物发生化学反应;4)注射器必须无菌,即在使用前应保持无菌状态,以避免感染,目前常见的方案为预灌封注射器。
图7:注射器分析-头部企业

资料来源:弗若斯特沙利文、源达信息证券研究所
3.产业链中游分析
政策合规要求、技术革新与自主研发能力、规模化生产能力以及不断变化的市场需求,共同构筑了产业链中游的发展壁垒。目前中游企业进入行业主要通过自主研发、外部收并购以及获取代理权三种形式。
图8:产业链中游竞争壁垒分析

资料来源:弗若斯特沙利文、源达信息证券研究所
行业发展壁垒主要在于:1)政策合规要求日趋严格:国家政府围绕原材料、终端产品乃至上市销售等环节,不断出台并完善相关法律法规及监督管理条例,行业合规化发展已成底层共识。日趋严格的政策法规也对企业的“合规化生产经营提出要求,具备合规基因的企业不易被快速更新迭代的市场淘汰;2)技术革新与自主研发能力:传统医美注射剂通过物理填充物填补凹陷除皱塑形,易出现馒化脸、交联剂残留等问题,再生类材料具有可通过产生/补充胶原蛋白等各种通路实现面部年轻化的功效迎合市场对非手术类医美需求增加的趋势。合成生物与重组胶原蛋白技术的发展,要求生产企业具备较强自主研发能力,从而以技术迭代优势屹立行业潮头;3)规模化生产能力:由于医美再生抗衰注射剂行业仍属于蓝海赛道,随着企业技术突破、产品优势被市场发现,未来下游市场需求的快速提升,也对企业规模化生产能力带来挑战。缺乏大规模投产能力,不具备相应的产能优势,就会限制注射剂产品在市场上的应用和推广速度,从而影响企业在终端市场的渗透速度和市场份额的扩大;4)响应市场需求:快速发展的行业将不断吸引更多的新进入市场参与者,未来行业的竞争态势将持续加剧,冲击现有竞争格局。市场对“抗衰”需求的不断提升,要求生产企业具备敏锐的商业嗅觉,积极响应不断变化的市场需求,从而实现公司产品的不断迭代创新。
4.产业链下游分析
消费者对机构或医生的专业性考量、医美机构的客户留存与拓新是下游市场最大痛点,近年中游厂商通过KOL教育不断增强中下游协同性,利于提高注射医生水平的同时,及时获得临床反馈,实现全产业链良性闭环。
医美高端需求人群认为不同医美机构或医生所擅长的项目不同,从而针对性地造访不同机构或医生,因此机构或医生的专业性将是消费者选择机构的重要因素。而从医美机构面临的挑战看,拓新难和客户流失严重是医美机构面临的最大挑战。中游厂商逐渐注重KOL教育,未来产业链中下游的协同性将不断增强;消费者对医美服务的质量和安全性要求日益提升,因此对注射医生的专业水平和注射经验提出了更高的要求但由于目前中国市场高水平的专业医生数量不足,因此近年诸多中游厂商通过举办注射会实操会、大师班等活动,为医生提供多维度、专业化的培训教育,将赋能注射医生诊疗水平的提升,同时也可及时获得临床反馈,利于推动行业的正规化、专业化发展。
图9:医美新客首诊机构选择
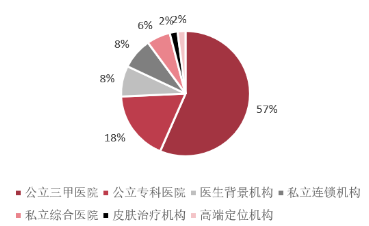
资料来源:《中国医美行业2024年度洞察报告》,弗若斯特沙利文,源达信息证券研究所
图10:医美机构面临的主要困难与调整
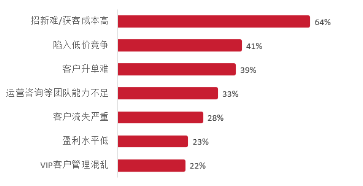
资料来源:《中国医美行业2024年度洞察报告》,弗若斯特沙利文,源达信息证券研究所
图11:企业加强中下游协同性举措

资料来源:弗若斯特沙利文,源达信息证券研究所
三、中国医美再生抗衰注射剂行业监管及政策
1.行业监管
国家卫生健康委员会、国家药品监督管理局以及市场监管总局,共同构成了中国医美再生抗衰注射剂行业的核心监管机构体系,从基础法规、研发注册、生产、销售宣传到产品使用各环节形成了监督管理的闭环。
图12:行业主要监管机构
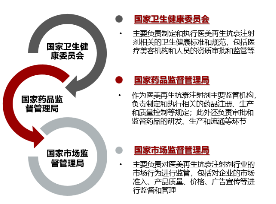
资料来源:弗若斯特沙利文,源达信息证券研究所
监管机构主要职能主要包括:1)制定基础法规:负责制定并监督实施覆盖医疗机构、医疗服务和医疗美容产品管理办法,明确分类标准与行业规范,确保产品与服务的安全性与合规性;2)研发注册:制定并实施医美产品研发与注册相关规范,明确注册审查的指导原则和命名规则,确保产品研发和注册过程的科学性、规范性和一致性;3)生产:制定并实施生产监管条例,明确委托人制度的具体要求,同时设立禁止委托生产目录,确保医美产品生产过程合法合规,质量安全可靠;4)销售宣传:制定广告管理办法,规范药械购销行为与互联网交易规则,确保销售宣传活动合法合规,防止虚假宣传及违规操作;5)产品使用:制定临床使用管理规范和服务管理条例,并完善从业人员培训大纲,确保医美产品使用安全合规,提升服务质量和从业人员的专业水平。
2.法律法规及行业政策
中国快速发展的医美市场,目前存在服务机构质量参差不齐产品定价混乱等行业不规范现象,近年通过从研发注册、生产、销售等各环节,颁布系列行业标准及政策法规,推动了行业进入“强监管时代”。进入“强监管时代”的中国医美市场,将提高产品取证上市的门槛,对生产企业的“合规化”经营提出更高要求从长期看也将推动医美再生抗衰注射剂行业的健康有序发展。
表1:医美再生抗衰注射剂行业基础法律法规
|
时间 |
发布机构 |
文件名称 |
主要内容 |
|
2021年3月 |
国务院 |
《医疗器械监督管理条例》 |
对医疗器械的生产、经营使用等各个方面做出规范。 |
|
2021年4月 |
NMPA |
《重组胶原蛋白类医疗产品分类界定原则》 |
规范重组胶原蛋白类医疗产品管理属性和管理类别判定。 |
|
2021年5月 |
NMPA等八部门 |
《关于印发打击非法医疗美容服务专项整治工作方案的通知》 |
关于在全国范围内开展打击非法医疗美容服务专项整治工作的任务包括:严厉打击非法开展医疗美容相关活动的行为;严格规范医疗美容服务行为;严厉打击非法制售药品医疗器械行为;严肃查处违法广告和互联网信息。 |
|
2022年1月 |
NMPA |
《重组胶原蛋白》 |
规定了重组胶原蛋白的质量控制要求、检测指标及检测方法等。 |
|
2022年03月 |
NMPA |
《医疗器械分类目录》 |
药品监督管理部门继续按照原受理类别审评审批,准予注册的核发医疗器械注册证。 |
|
2022年03月 |
市场监管总局 |
《医疗器械生产监督管理办法》 |
落实全面推行医疗器械注册人制度,完善监管手段。 |
|
2023年01月 |
NMPA |
《重组人源化胶原蛋白》 |
规定重组人源化胶原蛋白的质量控制、技术要求、试验方法、稳定性、生物学评价以及包装、运输和贮存等,适用于作为医疗器械原材料的不含非人胶原蛋白氨基酸序列的重组人源化胶原蛋白的质量控制。 |
|
2023年02月 |
NMPA |
《关于做好第三批实施医疗器械唯一标识工作的公告》 |
确定将部分临床需求量较大的一次性使用产品、集中带量采购中选产品、医疗美容相关产品等部分第二类医疗器械作为第三批医疗器械唯一标识实施品种。 |
|
2023年05月 |
国家卫健委等十四部门 |
《2023年纠正医药购销领域和医疗服务中不正之风工作要点》 |
要求健全完善行风治理体系,重点整治医药领域突出腐败问题,要点中表明深入治疗医疗领域乱想,树牢违法违规行为惩治高压线,聚焦医疗美容、口腔、辅助生殖等重点领域,依法依规严厉打击虚假宜传、无证行医、非法生产经营使用相关药品医疗器械等问题整治查处广告违法行为、违规开展诊疗服务,严格规范收费行为。 |
|
2023年05月 |
国家市场监管总局、公安部等十一部门联合印发 |
《关于进一步加强医疗美容行业监管工作的指导意见》 |
加强医疗美容行业监管工作,规范和促进医疗美容行业发展提出一系列针对性举措,其中明确规定医疗美容服务属于医疗活动,必须遵守卫生健康有关行业准入的法律法规。还明确要求将医疗美容诊疗活动、涉医疗美容经营活动以及医疗美容用药品医疗器械等纳入综合监管重点事项。 |
|
2024年01月 |
国务院办公厅 |
《关于发展银发经济增进老年人福祉的意见》 |
要发展抗衰老产业,深化皮肤衰老机理、人体老化模型、人体毛发健康等研究加强基因技术、再生医学、激光射频等在抗衰老领域的研发应用。 |
资料来源:弗若斯特沙利文,源达信息证券研究所
表2:医美再生抗衰注射剂行业研发注册、生产、销售宣传及使用法律法规
|
|
时间 |
发布机构 |
文件名称 |
主要内容 |
|
研发注册 |
2023年05月 |
国家药监局医疗器械技术审评中心 |
《重组胶原蛋白创面敷料注册审查指导原则》 |
本指导原则旨在指导注册申请人准备及撰写重组胶原蛋白创面敷料注册申报资料,同时也为技术审评部门审查注册申报资料提供参考。 |
|
2023年05月 |
国家药监局医疗器械技术审评中心 |
《重组人源化胶原蛋白原材料评价指导原则》 |
旨在指导注册申请人对医疗器械所用重组人源化胶原蛋白原材料进行充分的研究,并整理形成产品注册申报资料,同时也为技术审评部门对重组人源化胶原蛋白制成的产品注册申报资料包括所引用主文档相关内容的技术审评提供参考。 |
|
|
2023年04月 |
国家药监局医疗器械技术审评中心 |
《射频美容设备注册审查指导原则》 |
规范射频美容设备纳入医疗器械管理,其中要求,射频美容设备的适用范围描述应给出明确的应用部位、使用禁忌,鉴于射频美容设备的治疗有效性与能量强度存在直接的关联性,不同能量水平下的有效性需主要通过临床评价来证实。 |
|
|
2015年12月 |
原食品药品监管总局 |
《医疗器械通用名称命名规则》 |
医疗器械通用名不得出现绝对化、排他性词语,不得出现“美容”等宣传性词语。 |
|
|
生产 |
2022年03月 |
NMPA |
《禁止委托生产医疗器械目录》 |
整形填充材料、整形用注射填充物、乳房植入物等被列入禁止委托生产目录。 |
|
2022年03月 |
NMPA |
《医疗器械临床试验质量管理规范》 |
规定了医疗器械临床试验的程序要求,包括医疗器械临床试验的方案设计、实施、监查、稽查、检查以及数据的采集、记录、保存、分析,总结和报告等。 |
|
|
销售宣传 |
2023年4月 |
市场监管总局 |
《医疗美容消费服务合同》 |
医疗美容服务书面合同从无到有的突破,让医疗美容消费服务合同签订有据可依。 |
|
2023年02月 |
市场监管总局 |
《广告绝对化用语执法指南》 |
医疗美容广告中出现与疗效、治愈率、有效率等相关的绝对化用语的,一般不认为属于违法行为轻微或者社会危害性较小。 |
|
|
2022年10月 |
市场监管总局 |
《医疗美容行业虚假宣传和价格违法行为治理工作指引》 |
包括对虚假宣传和价格违法行为的监管措施,如现场检查、立案调查、信息公开等。 |
|
|
2021年11月 |
市场监管总局 |
《医疗美容广告执法指南》 |
从广告内容、社会风气等方面对医疗美容广告监管工作提供指引。 |
|
|
使用 |
2021年02月 |
NMPA |
《医疗器械临床使用管理办法》 |
对医疗器械的临床使用、保障维护、安全事件处理等做出规范。 |
资料来源:弗若斯特沙利文,源达信息证券研究所
四、中国医美再生抗衰注射剂行业发展环境
1.行业驱动因素
1)在银发经济、年轻消费者对抗衰老需求接受度提高的驱动下,市场对未来“抗衰”类产品发展看好,同时合成生物学技术与重组胶原蛋白技术的发展,也将加速产品的规模化、绿色化生产,促进降本增效。
医美再生抗衰注射剂行业的驱动因素有两个,一是抗衰类需求的提升,二是技术迭代推动发展。人口老龄化伴随下的银发经济,以及消费者健康需求深化下对抗衰老接受度提早影响下,未来“抗衰”类产品市场需求提振。
|
图13:中国65岁以上老年人人口数量占全国总人口比重 |
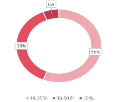
图14:中国购买抗衰老产品的消费者年龄画像 |
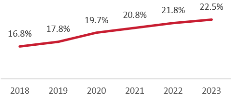
|
|
|
资料来源:国家统计局,《腾讯2024年度轻医美消费趋势白皮书》,弗若斯特沙利文,源达信息证券研究所 |
资料来源:国家统计局,《腾讯2024年度轻医美消费趋势白皮书》,弗若斯特沙利文,源达信息证券研究所 |
图15:非手术类医美消费需求日益理性,抗衰紧致是消费者首要需求
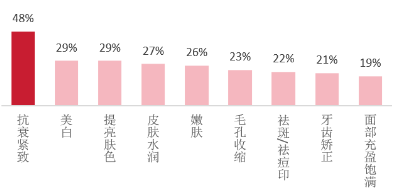
资料来源:国家统计局,《腾讯2024年度轻医美消费趋势白皮书》,弗若斯特沙利文,源达信息证券研究所
合成生物学技术对生物进行有目标地设计、改造或创造,赋予其非自然功能的“人造生命”,进而实现高效低碳地规模化生产、加工。合成生物学推动了生物医药、保健食品等多个行业的技术升级和市场扩展,赋能企业实现高附加值产品的商业化。重组胶原蛋白技术通过结构生物学和蛋白质理性设计实现规模化生产,推动了生物医用材料行业的升级,提高了材料的安全性和功能性,尤其是在医疗器械和功能护肤品领域,为市场提供了高生物活性、强稳定性的产品。
2)从美学观念变化、国民消费能力、医美市场渗透率看,人均GDP的增长提高了居民医美消费能力,并增强了居民的医美消费意愿,未来较低市场渗透率的中国医美市场有望迎来较快增长步伐。
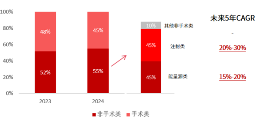
从美学观念变化看,非手术类市场中注射类市场具有较大增长空间。由于非手术类市场具有创面较小、风险较低、恢复期短、效果显著等特点,受到了越多的消费者选择,使得2024年其在医美市场的占比进一步增长至55%。其中注射类项目因其效果相对显著,且契合消费者美学观念变化的需求,其在所有非手术类医美市场份额达到45%。
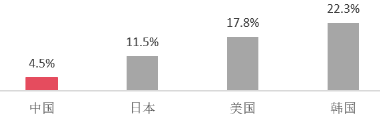
医美市场渗透率看,中国市场未来发展空间广大。2023年中国医美市场渗透率仅处于4.5%的水平,与韩国相差近5倍,未来会有至少2-5倍的市场增长空间。根据《中国医美行业2024年度洞察报告》显示,2023年有91%的需求者维持或增加了医美消费金额,预计66%需求者将继续维持或增加医美消费金额,因此医美消费意愿的提升将增加中国医美市场渗透率。
|
图16:中国医美细分市场占比及增速预测 |
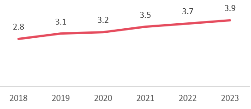
图17: 中国居民人均可支配收入 |
|
|
|
|
资料来源:弗若斯特沙利文,源达信息证券研究所 |
资料来源:弗若斯特沙利文,源达信息证券研究所 |
图18:2023年全球主要国家医美市场渗透率
资料来源:弗若斯特沙利文,源达信息证券研究所
2.行业制约因素
由于行业合规性提高、技术瓶颈仍需突破、市场竞争日趋激烈、消费者对产品的认知与信赖度的培育,使得目前市场存在产品供给不足、终端可及性、下游教育成本等的发展制约问题。
1)行业合规与市场监管趋于严格,提高企业获证门槛,市场供给不足。(i)行业合规性的提高:随着国家的市场监管政策逐步规范、收紧,医美再生抗衰注射剂产品也将面临更高的质量标准和更严格的审批流程。中国三类医疗器械的开发和注册周期通常在5-8年左右,这不仅对企业的运营能力提出要求,也延长了新产品从研发到市场的周期。(ii)市场供需关系下的产品供给不足:中国大陆市场起步较晚,且受到审批机制以及较高的研发创新与规模化生产的市场准入门槛影响,企业获证门槛较高,使得目前国产产品的市场供给不足。
2)研发创新与规模化生产难题,制约产品终端可及性和消费接受度。(i)技术瓶颈仍需不断突破:目前暴露的结节、肉芽肿问题,使得中游厂商仍需要突破相关技术难题,因此未来仍需要在新型材料的研发、生产工艺的优化、产品效果的持久性等方面进行突破。(ii)影响产品终端可及性:由于医美类产品的特有属性,对注射医生的操作手法具有较高的要求,因此基于目前所存在的高水平医生供给不足的发展现状,将影响产品的终端可及性,也带来消费者的信赖问题。
3)高速发展的市场增加未来新进入市场参与者,对企业综合能力提出更高要求。(i)市场发展仍处于早期:目前中国大陆地区已上市及主要在研的微球再生类产品多为童颜针,获批数量不多且多以模仿或引进海外成熟产品为主。从竞争现状看,价格战、虚假宣传等不正当竞争手段的使用,不仅损害了消费者的权益,也扰乱了市场发展的正常秩序。(ii)企业综合能力的提升成为市场破局关键:未来市场竞争将日趋激烈,企业间的竞争也将从单纯的产品竞争演变为全方位的渠道、品牌建设等多维度的实力较量。
4)消费者对产品的认知和医生的信赖,增加了市场教育成本。(i)消费者对产品的认知与信赖度的培育:新材料及新产品的出现,使得消费者对其的认知度仍需要时间进行培育。此外,消费者看重注射医生的操作手法以及注射经验,例如注射医生对材料特性的掌握,会影响童颜针复溶的均匀度,最终影响注射效果。(ii)中游企业对下游的教育成本增加:竞争激烈的市场环境下,企业需要推出迎合消费者需求的产品,因此也需要投入更多资源进行消费者教育和注射医生培训,提高其对医美再生抗衰注射剂的接受度和认知度。
五、中国医美再生抗衰注射剂行业竞争格局
1.医美再生抗衰注射剂上市及在研产品
胶原蛋白类产品因起步较早,目前拥有最多已上市产品数量,近年重组胶原蛋白是主要研究方向。PDRN类材料起步较晚,目前全球范围内仍以意大利、韩国企业为主流产品代表。
从全球市场格局看,由于全球医美再生抗衰注射剂市场起步于欧美及韩国,因此最早获批上市的产品也主要由这些国家的企业生产,近年中国本土企业在技术专利、收并购及产品引进的动作频繁,如巨子生物的重组胶原蛋白技术在中国获得行业内首个发明专利授权、华东医药收购拥有“少女针”伊妍仕产品的Sincair公司为其全资子公司、吴中美学引进的AestheFi艾塑菲为中国首款进口的童颜针产品,代表中国企业在全球市场奋起直追,行业影响力不断提高。
图19:医美再生抗衰注射剂的部分上市产品分析
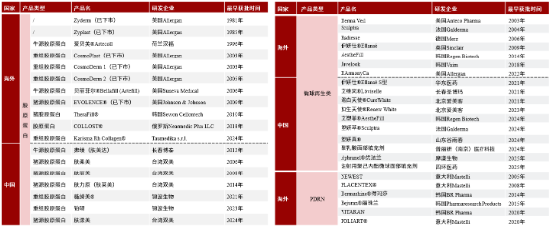
资料来源:弗若斯特沙利文,源达信息证券研究所
图20:医美再生抗衰注射剂的主要在研产品分析
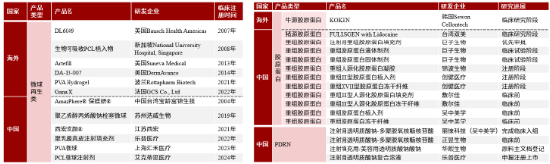
资料来源:弗若斯特沙利文,源达信息证券研究所
2.医美抗衰注射剂产品分析
Sculptra为第一代童颜针产品,凭借美国FDA核准及国际ISO认证的全新制程专利技术等优势,已实现在全球40多个国家和地区销售。艾维岚是第二代童颜针产品,已于2021年在中国大陆上市。Aestheri采用了最新的PDILA技术,且是国内唯一款获批的PDLLA材料的童颜针,目前已在全球68个国家和地区实现销售。Derma Veil是唯一由美国生产的PLLA注射物,但目前未在中国大陆实现销售。薇旖美是全球首款获得药监局批准的三类医疗器械批件的重组III型胶原蛋白植入剂,具有显著的先发优势和稀缺性。Reiuran凭借PDRN成分的安全有效性及效果,拥有较高市场地位。
具体来看:
1)Scylptra
产品介绍:在全球40多个国家和地区销售;由聚左旋乳酸、羧甲基纤维素钠和甘露醇组成,采用无菌加工工艺生产;主要用于真皮深层、皮下层注射,以矫正中面部容量缺失和/或中面部轮廓缺陷;建议进行2-3次注射,每次间隔4至6周,整个疗程所需的用量因人而异,3次疗程平均共需要3至6瓶,维持时间约25个月,但具体维持时间会因个人生活习惯、胶原蛋白流失速度而不同。
产品上市时间:1999年,欧洲获批用于面部容积缺失的填充治疗,2004年,美国FDA批准用于HIV阳性患者面部脂肪萎缩及双侧不对称矫正治疗,2010年,美国FDA批准用于健康人群的注射填充鼻唇沟以及其他面部深度皱纹,2023年,美国FDA批准可用于面颊部细纹和皱纹矫正,成为首个获得该适应症批准的PLLA型微球再生类材料。
产品优势:采用美国FDA核准及国际ISO认证的全新制程专利技术,富含100%聚左旋乳酸青春微粒,可刺激30倍以上自体胶原蛋白的制造,每一瓶4D舒颜萃约能增生3cc-4cc胶原蛋白,可帮助肌肤提升67%胶原蛋白新生,并能使皮肤增厚6.8mm。
2)艾维岚
产品介绍:主要由聚左旋乳酸(PLLA)、甘露醇和羟甲基纤维素钠(CMC)组成,主要适用于注射到真皮深层,以纠正中重度鼻唇沟皱纹。聚左旋乳酸具有生物可降解性,可逐步被人体自然分解,分解产物左旋乳酸可有效激发皮肤内成纤维细胞活力,并激活自身Ⅰ型及Ⅲ型胶原再生,提升皮肤紧致度,改善面部皱纹。
产品上市时间:2021年4月,获得NMPA的医疗器械注册证,成为国内第一款国家三类医疗器械的聚左旋乳酸PLLA“童颜针”产品,并于同年8月在中国大陆正式上市,2021年5月,获得欧盟CE认证。
产品优势:采用Ti-H系列专有技术,可控制微球在2年内匀速降解,实现体内稳定的胶原生长和较低的炎性反应,维持时间长达12-24个月。目前国内首家采用RFID射频识别技术的医美品牌,通过RFID芯片加密系统,保证产品从原料到成品,以及后续供应链每一个环节可追溯,为所有的医美医生与求美者从源头上保证产品的科学性。采用的核心成分聚左旋乳酸(PLLA)是人体内源性物质,具有良好的生物相容性,在体内最终会被代谢为二氧化碳和水,不会残留在身体里造成负担,安全性高。
3)艾塑菲
产品介绍:为第三代童颜针,采用最新PDLLA技术,且是国内唯一一款获批的PDLLA材料的童颜针。为PDLLA微球和羧甲基纤维素钠组成的冻干粉,使用前需经灭菌注射用水复溶为混悬液,用于注射到面部真皮深层,以纠正中重度鼻唇沟皱纹。
产品上市时间:2014年,在韩国获批上市,2019年,在中国台湾获批上市,2024年,获得NMPA注册证,进入中国大陆地区。
产品优势:2024年国际童颜针品牌中AestheFill全球终端销售额排名第一,市占率约为28%;多孔海绵状的微球设计给产品带来“百变”特性,超高浓度复溶提供骨性支撑,较高浓度复溶提供容量提升,低浓度提供软组织年轻化。全球68个国家和地区10余年的临床探索,从骨膜到真皮各不同层次均有丰富的应用经验,可“百搭”联合其他注射类产品或光电仪器、手术等治疗手段,带给求美者最精准的美容定制化服务。聚双旋乳酸的原料选择,环境友好、组织相容性好、可完全降解(代谢产物二氧化碳和水),材料降解时间更适中(12~16个月),美容效果维持时间仍优异(24个月)。
4)Derma Veil
产品介绍:在美国、韩国、拉丁美洲、远东、东南亚销售(中国大陆未上市),突破传统自体胶原增生技术的局部塑形局限,新增了天然果酸甘醇酸成分,其微小分子易于渗透,有效促进表皮层变得幼嫩且增厚,强化肌肤支撑力,使肌肤触感柔软、丰盈有弹性,同时注入水分,倍增美白润泽效果,适用于面部任何部位,全脸塑造均匀的轮廓,注射后效果会在2周内逐渐显现,效果通常可维持2年或以上。
产品上市时间:2003年,获得墨西哥卫生部(SSA)认证;2006年,广泛用于拉丁美洲及远东至东南亚地区。
产品优势:由美国Anteco Pharma生产,符合药品优良制造标准(cGMP) 和ISO7等级卫生标准,是唯一由美国生产的PLLA注射物,有效实现肤质嫩白再生、重塑年轻轮廓、自然逆转肌龄的效果,且注射后不易结块或出现微粒,填充物形态改为不规则颗粒,适合面部不同位置的塑形效果更准确,更理想。
5)薇旖美
产品介绍:目前主要在中国市场销售,已覆盖全国超2,000家医疗机构。主要用于面部真皮组织填充以纠正额部动力性皱纹(包括眉间纹、额头纹和鱼尾纹)。
产品上市时间:2021年,在中国大陆获批上市,2024年,获越南医疗器械注册证。
产品优势:核心成分是重组Ⅲ型人源化胶原蛋白,与人体自身的胶原蛋白结构高度相似,消除了胶原蛋白免疫原性,具有与人体胶原蛋白一样的三螺旋结构,生物相容性好,注射后不易引起过敏反应。采用NSA纳米微距自组装技术,将多个三螺旋结构组成非常稳定的致密胶原纤维结构,2.5倍活性胶原纤维,可以牢牢束紧胶原蛋白网。
6)Rejuran
产品介绍:在亚洲、北美、欧洲和中东等30多个国家和地区销售,主要成分是cPDRN再生修复因子,有助于推迟老化、促进肌肤健康度、提升肌肤表面屏障与修复脆弱肤况。基于包含不同的成分而拥有不同版本,如透明质酸(HA)和利多卡因,以增强保湿效果和减少注射时的疼痛感。
产品上市时间:2014年,在韩国获批上市,未在中国大陆获批。
产品优势:采用独家专利技术DOT,能使肌肤厚度增加,强化肌肤屏障,可抵御环境及非环境因素引起的肌肤早衰现象。术后4周,皮肤真皮层的密度及厚度增加(15%~30%),利用C-PDRN、医用级玻尿酸和泛醇等成分,产品能有效修复受损细胞,发挥抗炎和抗氧化作用,改善痘痘肌和敏感肌,并提高皮肤修复和再生能力,从而强化皮肤屏障并恢复肌肤健康状态,通过其主要成分多核苷酸在皮肤再生和修复方面表现出色,适用于多个部位,包括全脸、颈部、锁骨、手背、眼周和T字区。
六、中国医美再生抗衰注射剂行业发展趋势
1.需求端发展趋势
人口老龄化提振的抗衰需求、非手术类医美是中高收入医美消费者的主流项目选择、消费者美学观念向轻量化项目转变以及对注射部位的需求转变,将推动生产企业在开发注射剂产品时,更关注功能及功效。
|
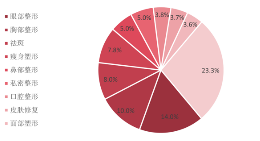
图21:2024H1医美细分项目咨询占比 |
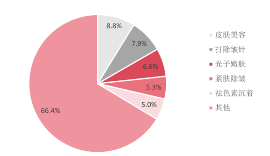
图22:皮肤美容消费侧细分咨询项目分布 |
|
|
|
|
|
|
资料来源:弗若斯特沙利文,源达信息证券研究所 |
资料来源:弗若斯特沙利文,源达信息证券研究所 |
|
图23:2024计划增加投入项目vs 2023年治疗项目

资料来源:弗若斯特沙利文,源达信息证券研究所
消费者美学观念以及功效需求的变化,推动具备“抗衰”功能的注射剂市场发展。目前中高收入医美消费者中,非手术类医美项目仍是其主流的项目需求,消费者美学观念正逐步向轻量化医美项目转变,消费者的审美追求更自然。此外,根据对近3000万医美消费者于2024年上半年度的搜索数据显示,“皮肤美容”类项目连续三年占比前二,人们对皮肤美容的需求不断增长,尤其是在面部年轻化、抗衰除皱等方面的需求。注射部位未来将从面部拓展至身体部位,私密整形项目从2023年占比第十一名提升至第七名,未来也将推出更对针对身体部位的注射剂产品,以迎合不断变化的消费者需求。
2.供给端发展趋势
新技术和新材料的迭代与出现,将提供在胶原蛋白生成速度、维持时效、可降解性以及个性化定制等方面优势的注射剂产品,未来有望逐步替代传统医美注射材料的部分市场空间。
图24:部分医美材料生命周期表
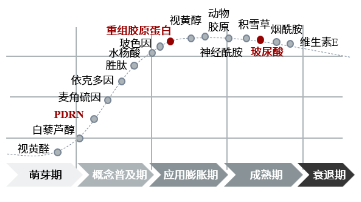
资料来源:弗若斯特沙利文,源达信息证券研究所
玻尿酸填充注射剂市场发展成熟且竞争激烈。2024年,玻尿酸三类器械产品获批数量超70个,市场竞争十分激烈,目前应用场景涵盖了功能性护肤品、食品、洗发水、漱口水等。此外,玻尿酸填充注射剂存在维持时效短、易移位、不易被完全降解代谢和吸收等劣势。
1)趋势一:技术面
以重组胶原蛋白类材料为例,企业通过持续开发更先进的制剂工艺和交联技术,以更好地提高产品的稳定性和持久性,减少过敏反应,提供更好的填充效果。
表3:技术面优势
|
企业 |
相关技术 |
技术优势 |
|
巨子生物 |
无交联剂残留的交联技术 |
使用碳二亚胺对大分子I型重组胶原蛋白进行交联,所用的交联剂浓度低,操作简单易行可通过二次交联提高交联度,且交联反应完成后仅通过简单的磷酸缓冲液清洗操作即可基本完全除去碳二亚胺。 |
|
美柏生物 |
利用化学催化剂将胶原蛋白和玻尿酸进行交联 |
不仅增强了支撑性,还具有优异的细胞粘附能力,能促进细胞迁移与增殖,加速组织再生;材料在植入后7天快速促进细胞生长,28天开始降解,并在两个月内完全降解,展现出良好的生物相容性和组织修复性能 |
资料来源:弗若斯特沙利文,源达信息证券研究所
2)趋势二:材料面
玻尿酸材料因起步时间早,已成为红海市场,因此未来如PCL、PLLA等高分子材料的发展与革新,有望为行业带来增量空间,以羟基磷灰石为例:
表4:材料面优势
|
材料优势 |
中国市场研究现状 |
|
注射后羟基磷灰石晶球会形成一个骨架,促进胶原蛋白新生,并与羟基磷灰石晶球交错镶嵌在组织中,形成较稳固而柔软的结构。 |
2023年,Radiesse 启动“纠正中重度异唇沟皱纹”适应症的国内注册临床 2024年,艾尔建美学HArmonyCa““已在中国完成注册检验,即将展开临床试验 2024年,杭州协合医疗旗下重磅医美新品注射用羟基磷灰石复合填充Singderm“Dual“美神针”于欧洲首发 |
资料来源:弗若斯特沙利文,源达信息证券研究所
3)趋势三:联合疗法
因为技术革新突破、消费者需求变化、部分材料性能缺陷等因素,近年联合疗法兴起,厂商通过“玻尿酸+聚乳酸微球”,“玻尿酸+PDRN”材料的结合,推出功能更多样化的产品,也有利于推动较老医美材料的持续性商业化增长。
七、投资建议
行业企业的业务布局在趋于严格的行业合规与市场监管、较高壁垒的研发创新与规模化生产等市场痛点下,具有“合规化”基因,研产销全产业链布局,丰富产品布局的企业有望屹立快速发展的行业潮头,展现较强的发展潜力和投资价值。
图25:医美再生抗衰注射剂行业企业的业务布局
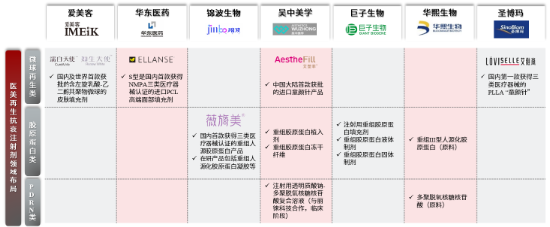
资料来源:弗若斯特沙利文,源达信息证券研究所
2.标杆企业
锦波生物锦波生物是国内重组胶原蛋白领头羊,其先发优势明显。2025年4月9日,其自主研发生产的全球首个“注射用重组Ⅲ型人源化胶原蛋白凝胶”正式获得国家药品监督管理局批准上市。目前公司在国内共获批3款重组胶原蛋白三类械产品,搭建全剂型产品矩阵(溶液、凝胶、固体),进一步打开产品应用场景,强化品牌建设。截至2024年末,已覆盖终端医疗机构约 4,000 家。
公司2024全年营收14.43亿元,同比增加84.92%,归母净利润7.32亿元,同比增加144.3,扣非归母净利7.12亿,同比增加149.2%。
|
图26:锦波生物营收及增速 |
图27:锦波生物归母净利润及增速 |
|
|
|
|
资料来源:Wind,源达信息证券研究所 |
资料来源:Wind,源达信息证券研究所 |
2020年至2024公司毛利率持续快速增长,分别为80.01%、82.29%、85.44%、90.16%、92.02%。原因主要为高毛利率的重组胶原蛋白医疗器械类产品销售收入迅速增长。锦波生物24年归母净利率50.75%,同比增加12.3%。高毛利业务收入占比提升以及期间费用率优化带动净利率提升。
|
图28:锦波生物毛利率与净利率 |
图29:锦波生物期间费用率 |
|
|
|
|
资料来源:Wind,源达信息证券研究所 |
资料来源:Wind,源达信息证券研究所 |
锦波生物2024年公司经营性现金流净额达7.67亿元,同比增长近1.6倍,经营活动现金流净额/归母净利润比率达1.05,验证盈利质量的高含金量。
|
图30:锦波生物现金流净额 |
图31:锦波生物归母净利润与经营活动现金流净额对比 |
|
|
|
|
资料来源:Wind,源达信息证券研究所 |
资料来源:Wind,源达信息证券研究所 |
此外公司预计推出股权激励,彰显公司发展信心。根据股权激励计划,向包括4位高管在内的87 人以276元/份授予100万份,业绩考核目标为2025-2027 年剔除股权激励费用后的扣非归母净利润分别不低于10/14/18亿元。
华东医药华东医药成立于1993年,历经30余年的发展,公司业务覆盖医药全产业链,拥有医药工业、医药商业、医美、工业微生物四大业务板块,已发展成为医药创新研发、生产、经销为一体的大型综合性医药上市公司。
公司目前在研全球创新产品十余款,融合“无创+微创”、“面部+身体”、“产品+技术”、“注射+能量源设备”等多元化联合治疗手段,在注射类产品实现再生类、玻尿酸和肉毒素三大品类的全覆盖并形成差异化管线。差异化创新产品管线和多元化业务板块,保障公司稳健发展。
2024年华东医药营收419.06亿元,同比增长3.16%,实现归母净利润35.12亿元,同比增长23.72%,实现扣非归母净利润33.52亿元,同比增长22.48%。公司自上市以来收入及利润增速始终维持稳健增长, 2020-2021年受到集采等因素影响,收入及利润增速首次出现回落。近几年,公司积极推进战略转型,加大研发投入,不断丰富产品管线及业务板块,收入及利润增速呈现逐步恢复态势。
|
图32:华东医药营收及增速 |
图33:华东医药归母净利润及增速 |
|
|
|
|
资料来源:Wind,源达信息证券研究所 |
资料来源:Wind,源达信息证券研究所 |
公司毛利率与净利率整体较为平稳,近几年呈现出缓慢上升态势。2024年公司研发费用14.26亿元,同比增长12.19%,增加了1.55亿元。目前公司将创新药业务作为战略重点方向,公司医药在研项目合计133个,其中创新药及生物类似药项目94个。
|
图34:华东医药毛利率与净利率 |
图35:华东医药研发费用率(%) |
|
|
|
|
资料来源:Wind,源达信息证券研究所 |
资料来源:Wind,源达信息证券研究所 |
2024年公司经营性现金流净额37.49亿元,同比略有下降。经营活动现金流净额/归母净利润比率达1.07,盈利质量良好。
|
图36:华东医药现金流净额 |
图37:华东医药归母净利润与经营活动现金流净额对比 |
|
|
|
|
资料来源:Wind,源达信息证券研究所 |
资料来源:Wind,源达信息证券研究所 |
3.行业重点公司一致盈利预测
|
公司 |
代码 |
归母净利润(亿元) |
PE |
总市值(亿元) |
||||
|
2024E |
2025E |
2026E |
2024E |
2025E |
2026E |
|||
|
锦波生物 |
832982.BJ |
11.0 |
14.7 |
19.7 |
37.2 |
27.7 |
20.7 |
408.0 |
|
华东医药 |
000963.SZ |
40.4 |
46.1 |
51.9 |
18.8 |
16.5 |
14.7 |
761.3 |
八、风险提示
政策变动风险;
行业竞争加剧;
新品研发不及预期。
 海量资讯、精准解读,尽在新浪财经APP
海量资讯、精准解读,尽在新浪财经APP
责任编辑:刘万里 SF014